Блог
Садыков С. А.
ИЗОТОПНЫЙ СОСТАВ УГЛЕРОДА В ЭЛЕМЕНТАХ АНАТОМИИ КРИСТАЛЛОВ КАЛЬЦИТА
Согласно принципу П. Кюри элементы симметрии строения формируют симметрию физико-химических свойств кристалла. Возможно, действие данного принципа локально меняет физико-химические параметры флюида окружающего кристалл. Как следствие, меняется взаимодействие карбонат-ионов, имеющих разный изотопный состав, с растущим кристаллом, что приводит к дополнительному фракционированию изотопов на гранях кристалла. Именно с анизотропностью свойств кристалла мы связываем чередование значений отношения стабильных изотопов углерода на гранях исследованных образцов кристаллов кальцита.
ИЗОТОПНЫЙ СОСТАВ УГЛЕРОДА В ЭЛЕМЕНТАХ АНАТОМИИ КРИСТАЛЛОВ КАЛЬЦИТА
С. А. Садыков
Институт минералогии УрО РАН, г.Миасс,
Конституция, т.е. взаимосвязанные химический состав и структура, есть сущность каждого минерала: атомы, соединившиеся в соответствующую структуру, это и есть минерал – природное химическое вещество и физическое тело [Григорьев, 1966]. Минерал [фр., mineral, лат. minera – руда] – физически и химически индивидуализированное тело, возникающее в результате естественных физико-химических процессов в земной коре; большинство минералов – твердые кристаллические соединения, приблизительно однородные по химическому составу и физическим свойствам; являются составными частями руд, горных пород и других геологических тел. Кристалл – тело (твердое или жидкое), частицы которого (атомы, ионы или молекулы) расположены в определенном, периодически повторяющемся порядке, образуя пространственную кристаллическую решетку. Свойства кристаллов: анизотропность, способность самоограняться, симметрия. Исходя из определений видно, что понятие кристалла является подчиненным по отношению к минералу. Минералы не всегда могут иметь вид и структуру кристалла (нефть, углеводороды, стекла). Минералы состоят из атомов химических элементов. Минерал как целое получает свои, специфические качества, принципиально отличающиеся от качеств каждого из составляющих его атомов и не сводящиеся к простой сумме таковых. Если еще учесть, что химические элементы состоят из набора изотопов, то возникает вопрос существует ли связь между структурой, свойствами минерала (или кристалла) и изотопным составом?
Объектом исследований были кристаллы кальцита из Дальнегорского скарново-полиметалического месторождения (Тетюхе), Приморский край.
Изотопный состав образцов определялся на масс-спектрометре Delta+ Advantage фирмы Thermo Finnigan. Ошибка измерений данных составляла 0,079 ‰, PDB.
В связи с длительной геологической историей Дальнегорских месторождений следует предположить, что при образовании кристаллов кальцита углерод использовался из 4-х источников: известняки (-1,09 ‰, PDB), графит (-23,18 ‰, PDB), растворенная в воде углекислота, атмосферный углекислый газ ( от -7 до -10 ‰, PDB). Ещё одним источником мог быть метан, идущий по трещинам из нижележащих горных пород.
Было исследовано 10 крупнокристалических образцов кальцита, разных форм. Семь образцов представляют собой гексагональные призмы, один образец – развитый ромбоэдр {02-21} с матовой поверхностью и узкими гранями спайного ромбоэдра, ещё один из образцов ромбоэдр (выколок по спайности), и последний, скаленоэдр ограниченный ромбоэдром. Отбор проб проводился с разных граней кристаллов и из разных частей кристаллов. Значение отношения стабильных изотопов углерода в исследованных образцах имеют значения от -8,64 до -34,33 ‰, PDB. В трёх образцах гексагональных призм, каждая из которых была распилена на несколько частей, выявлено изменение отношения изотопов по длине образца.
Все исследованные образцы отличаются своими изотопными составами от любого из вышеперечисленных источников углерода, т.е. при росте кристаллов происходило смешение углерода из разных источников. Неоднородность зонального образца кристалла кальцита, описанного нами в статье [Садыков и др., 2007], можно объяснить разными условиями роста зон. В трёх образцах кальцита призматической формы можно предположить, что негомогенность отношения изотопов возникла в процессе образования призмы за счет торможения слоев роста ромбоэдра и скаленоэдра (рис. 1). В образце призмы ограниченной папиршпатом также наблюдается неоднородность изотопного состава на гранях призмы. Исследования проб отобранных с граней ромбоэдра или скаленоэдра также показали неодинаковые значения изотопного состава. В одном из образцов имеется распределение стабильных изотопов углерода совпадающие с симметрией образца (тригональное распределение изотопов) (рис. 2.).
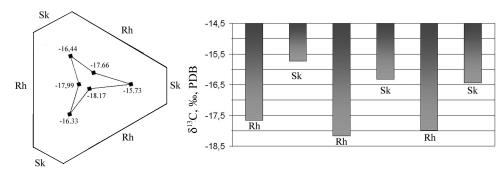
Рис. 1. Схема образования призмы при росте кристалла кальцита. а) идеальная форма кристалла, пунктиром нанесена линия разреза, b) схема поперечного разреза.
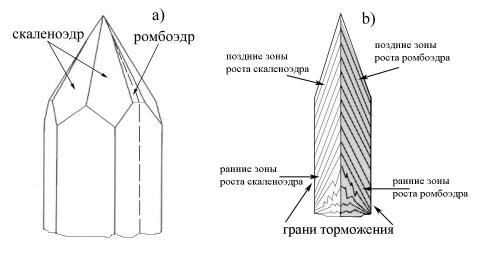
Рис. 2. Диаграмма распределения δ13С по граням в основании кристалла кальцита. Sk – грани скаленоэдра, Rh – грани ромбоэдра.
Ёще одним фактором, определяющим разницу значений отношений изотопов, является большая площадь отбора проб. Размер площадки пробы достигал 5 мм, глубина отбора также не регулировалась. Оптические исследования показали, что в кристаллах наблюдается тонкая зональность (толщинка зонок равна 10 мкм). При отборе проб попадал материал разных зонок и вициналей. Вероятно, исследования проведенные с использованием более локальных методов (лазерная абляция и т.п.) позволят уточнить полученные данные. Однако, во всех изученных кристаллах изотопный состав на разных гранях неодинаков и значительно превышает ошибки измерений.
Изотопный состав углерода карбонатов, осажденных из водных растворов, определяется следующими факторами [Фор, 1989]: 1) значением δ13С газообразной CO2, находящейся в равновесии с карбонатными и бикарбонатными ионами в растворе, 2) фракционированием изотопов углерода между газообразной CO2, карбонатными и бикарбонатными ионами в растворе и твердым карбонатом, 3) температурой, при которой устанавливается равновесие, pH и другими химическими свойствами системы. Вышеперечисленные параметры определяют энергетическую составляющую химических реакций при образовании карбонатов, в том числе и реакций изотопного обмена. Эти параметры являются внешними факторами по отношению к растущему кристаллу. В самом кристалле формируется так называемое “кристаллическое поле”. Это определяется взаимодействиями между ионами, атомами или молекулами внутри кристалла. Кристаллы обладают анизотропностью. Соответственно, поле внутри кристалла также анизотропно. На границе растущего кристалла происходит взаимодействие внешних параметров и “кристаллического поля”. Это взаимодействие находится в динамическом равновесии. Из квантово-механических расчетов следует, что энергия молекул или ионов с разным изотопным составом отличаются, хотя и не сильно. Т.е., свойства изотопов подобны, но не тождественны. Из-за анизотропности кристалла, молекулы или ионы с разными изотопными составами по-разному взаимодействуют на гранях с кристаллом. Поэтому происходит дополнительное фракционирование изотопов на гранях кристаллов.
Таким образом, на процесс фракционирования изотопного состава углерода при росте кристаллов кальцита влияют не только условия среды и вещественный состав флюида, но и процесс локального изменения среды на границе кристалл-среда, то есть кристаллы дополнительно фракционируют изотопы углерода на гранях.
Автор благодарен за помощь при проведении исследований В. Н. Анфилогову, В. А. Попову и Т. П. Нишанбаеву.
Литература:
1. Григорьев Д. П. Основы конституции минералов. М.: Недра, 1966, 76с.
2. Садыков С. А., Попов В. А., Анфилогов В. Н., Нишанбаев Т. П. Зональное распределение изотопов углерода в кристаллах гипергенного кальцита месторождений Дальнегорска, Приморский край. ДАН, 2007, том 412, № 2, 250-252.
3. Г. Фор. Основы изотопной геологии. М.: Недра, 590с.
